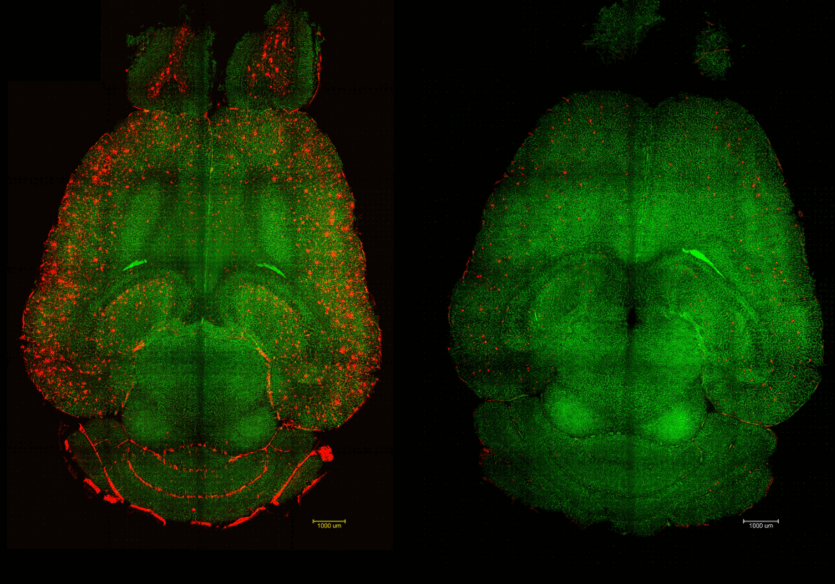
Протягом десятків років науковці різними способами намагались приборкати хворобу Альцгеймера, яка вважалась невиліковною. Новий прорив нарешті дозволив позбавитись цього вікового захворювання внаслідок буквально одного уколу.
Більшість наявних препаратів впливає безпосередньо на бета-амілоїдні білки, які накопичуються у мозку. Однак такий підхід демонструє доволі обмежені результати. Замість цього міжнародна група дослідників вирішила перезавантажити систему самоочищення у мозку.
Вчені використали наночастинки для відновлення функції гематоенцефалічного бар’єра, отримавши дивовижні результати. Буквально за 2 години вдалось очистити мозок мишей з прогресуючою хворобою Альцгеймера від майже половини амелоїдних бляшок.
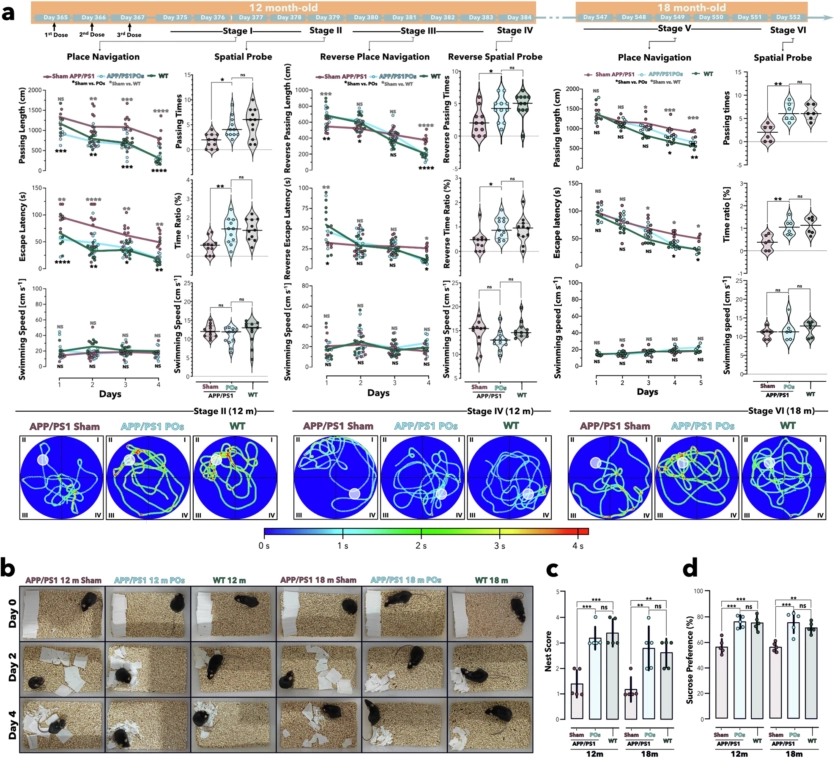
При цьому відновлення когнітивних функцій зберігалось. У хворих мишей відновилась пам’ять та здатність до навчання на рівні зі здоровими особинами. Покращені показники зберігались щонайменше пів року після одноразового лікування.
Оскільки мозок надзвичайно чутливий орган, він потребує серйозного захисту від токсинів та патогенів. Гематоенцефалічний бар’єр перевіряє кожну молекулу і пропускає лише поживні речовини. Окрім цього цей бар’єр також здійснює “прибирання”, позбавляючись від бета-амілоїдних білків. Однак у разі хвороби Альцгеймера ця система виходить з ладу.
Бета-амілоїдні білки накопичуються та призводять до руйнації мозкових тканин, викликаючи запалення та порушуючи зв’язок між нейронами. Врешті-решт, це закінчується тим, що клітини мозку починають вмирати.
Протягом багатьох років науковці розглядали порушення роботи гематоенцефалічного бар’єра як ознаку пізньої стадії розвитку хвороби Альцгеймера. Однак з’являється все більше даних про те, що таке уявлення помилкове. Порушення роботи цього бар’єру може відбуватись одним з перших під час хвороби Альцгеймера, що запускає подальші катастрофічні наслідки.
“Більшість сучасних методів лікування хвороби Альцгеймера спрямовані на видалення бета-амілоїду або захист нейронів після того, як пошкодження вже сталося. Але на цей момент захисний бар’єр мозку вже руйнується; він більше не може належним чином доставляти поживні речовини та виводити відходи. Ми прагнемо відновити цей бар’єр, оскільки він є основою проблеми. Здоровий гематоенцефалічний бар’єр підтримує клітини мозку, регулює запалення і підтримує середовище, необхідне нейронам для функціонування. Відновлюючи судинну мережу, ми допомагаємо мозку відновити природний баланс, роблячи будь-яку іншу терапію більш ефективною та тривалою”, — пояснює автор дослідження Джузеппе Батталья.
Відновлення гематоенцефалічного бар’єра непроста задача. У мозку міститься близько мільярда капілярів, утворюючи складну систему з високим рівнем безпеки. Ключову роль у цій системі відіграє білок LRP1, який чистить мозок від токсичних бета-амілоїдних білків. У людей з хворобою Альцгеймера вироблення цього білка різко знижується, а ті LRP1, що залишились, руйнуються під впливом бета-амілоїдних білків.
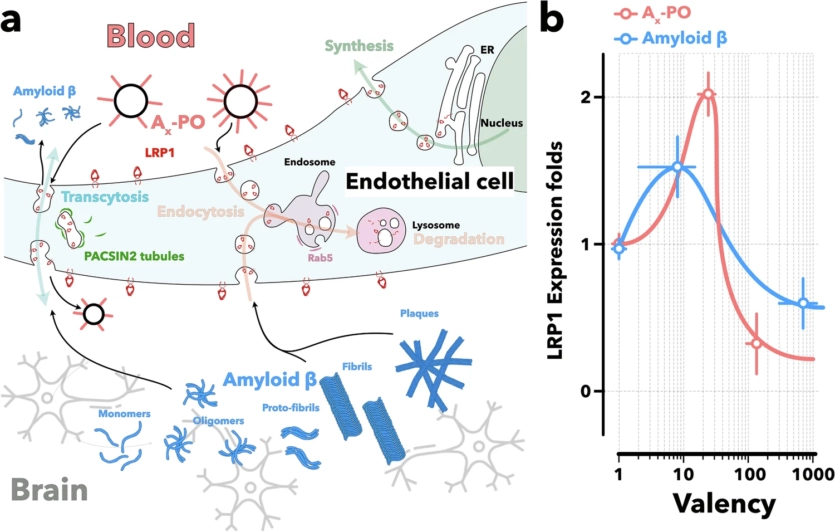
Для розв’язання цієї проблеми Джузеппе Батталья та його колеги створили інтелектуальну систему доставки — крихітну синтетичну сферу, яка називається полімерсомою. Ця частинка являє собою велику кількість різних компонентів, що працюють разом.
“Замість того, щоб використовувати одну активну молекулу, як у традиційних препаратах, наші наночастинки складаються з безлічі невеликих компонентів, які збираються подібно до будівельних блоків. Ці компоненти працюють спільно, не лише доставляючи ліки, а й ефективно взаємодіючи з гематоенцефалічним бар’єром. Саме тому ми називаємо їх “супрамолекулярними препаратами”: вони діють через структуру та взаємодію, допомагаючи власним клітинам мозку перезапустити процеси, що припинилися при хворобі Альцгеймера”, — розповідає Батталья.
Дослідники вкрили поверхню полімерсоми спеціальним пептидом, який зв’язується з білками LRP1 внаслідок мультівалентності. Недостатня кількість цього пептиду робила синтетичну частинку неефективною, а надмірна — подібною до бета-амілоїдних білків, зв’язуючи занадто сильно. З рештою вчені додали 40 пептидів на частинку, а після протестували на мишах із хворобою Альцгеймера.
У дослідженні брали участь миші віком близько року, генетично модифіковані для розвитку агресивної форми, схожої із хворобою Альцгеймера. Миші були старими, а їхній мозок був вкритий бета-амілоїдними білками, викликаючи значні когнітивні порушення. Буквально через 2 години після єдиного уколу концентрація бета-амілоїдів у мозку мишей знизилась майже на 45%.
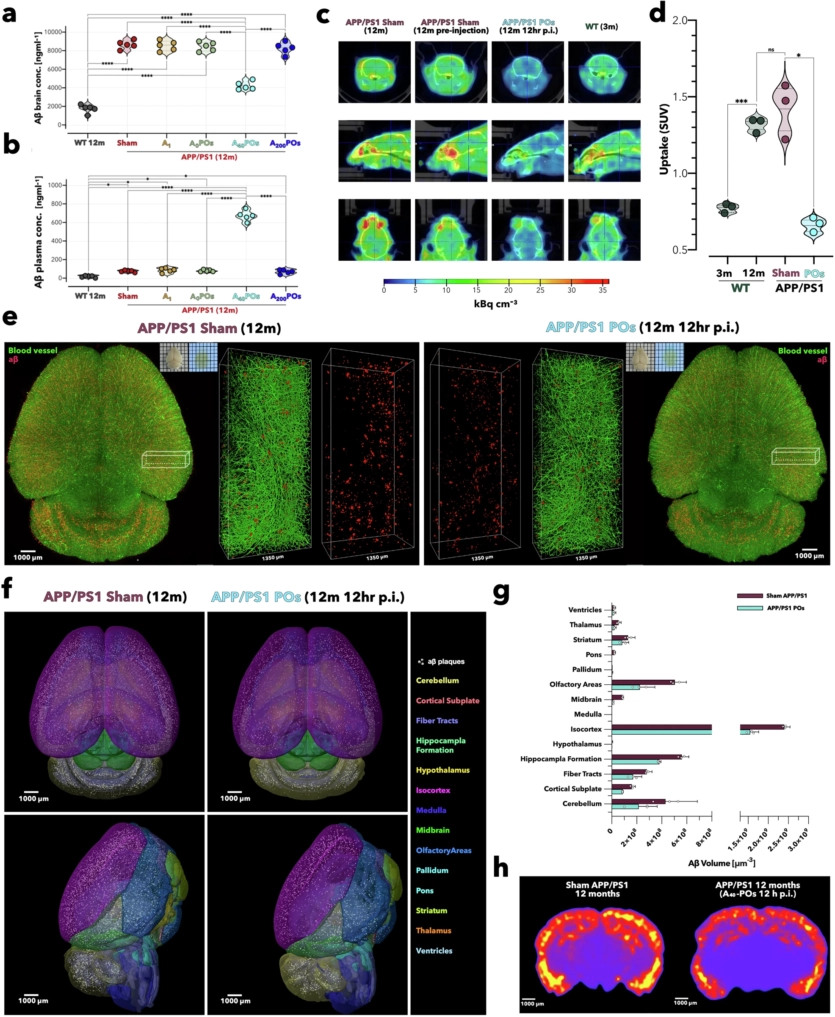
Концентрація бета-амілоїдів знижувалась не тільки у мозку, а й у плазмі крові. Це свідчило про те, що токсичні білки з мозку потрапляли в організм для утилізації. Кількість бета-амілоїду, виведеного з мозку, практично повністю відповідала його надлишку в крові. Результати зберігались через 6 місяців після ін’єкції.
“Результати виявилися напрочуд стійкими. Швидке зниження рівня амілоїду показує, що після відновлення транспортної системи бар’єра мозок може ефективно виводити самостійно шкідливі білки. Навіть через місяці ми спостерігаємо покращення пам’яті та функцій мозку у тварин, які пройшли лікування. Це говорить про те, що реактивація природних механізмів відновлення мозку може мати довгострокові переваги, а не лише тимчасові”, — зазначає Батталья.
Наступними кроками дослідників буде підтвердження безпеки їхнього методу та відтворюваність на більших за розмірами тваринах, проведення докладних токсикологічних досліджень відповідно до нормативних стандартів. Тільки після цього можна буде переходити до ранніх клінічних випробувань. Мета – перенести цей підхід з лабораторії на пацієнтів, запропонувавши новий спосіб лікування хвороби Альцгеймера, відновлюючи власні захисні та відновлювальні системи мозку.
Результати дослідження опубліковані у журналі Nature
Джерело: ZME Science






Повідомити про помилку
Текст, який буде надіслано нашим редакторам: